

近日,我校细胞治疗药物产业学院施明教授团队在 Frontiers in Immunology 杂志(中科院二区期刊,IF=5.7)发表题为“Advances in CAR optimization strategies based on CD28”的文章。施明教授、郑骏年教授和刘丹副教授为共同通讯作者,青年教师李思瑾和硕士研究生周雨思为共同第一作者。
CAR-T疗法作为癌症治疗领域的“明星疗法”,在血液系统肿瘤治疗中成效显著。然而,目前广泛应用的以CD28为共刺激分子的CAR-T细胞,在临床实践中面临诸多挑战,像治疗后复发率高、疗效持久性差,以及会引发严重不良反应等,限制了CAR-T疗法的进一步应用。研究团队深入剖析了CD28信号转导功能及CD28共刺激分子在CAR-T应用中存在的问题。CD28信号基序通过激活下游信号通路,调节T细胞激活、分化等功能,但使用CD28作为共刺激分子的CAR-T细胞会诱导较高水平的细胞因子释放,引发细胞因子释放综合征及神经毒性,还会导致CAR-T细胞代谢重编程,使其向效应T细胞分化,减少记忆T细胞比例,影响抗肿瘤活性和体内持久性。
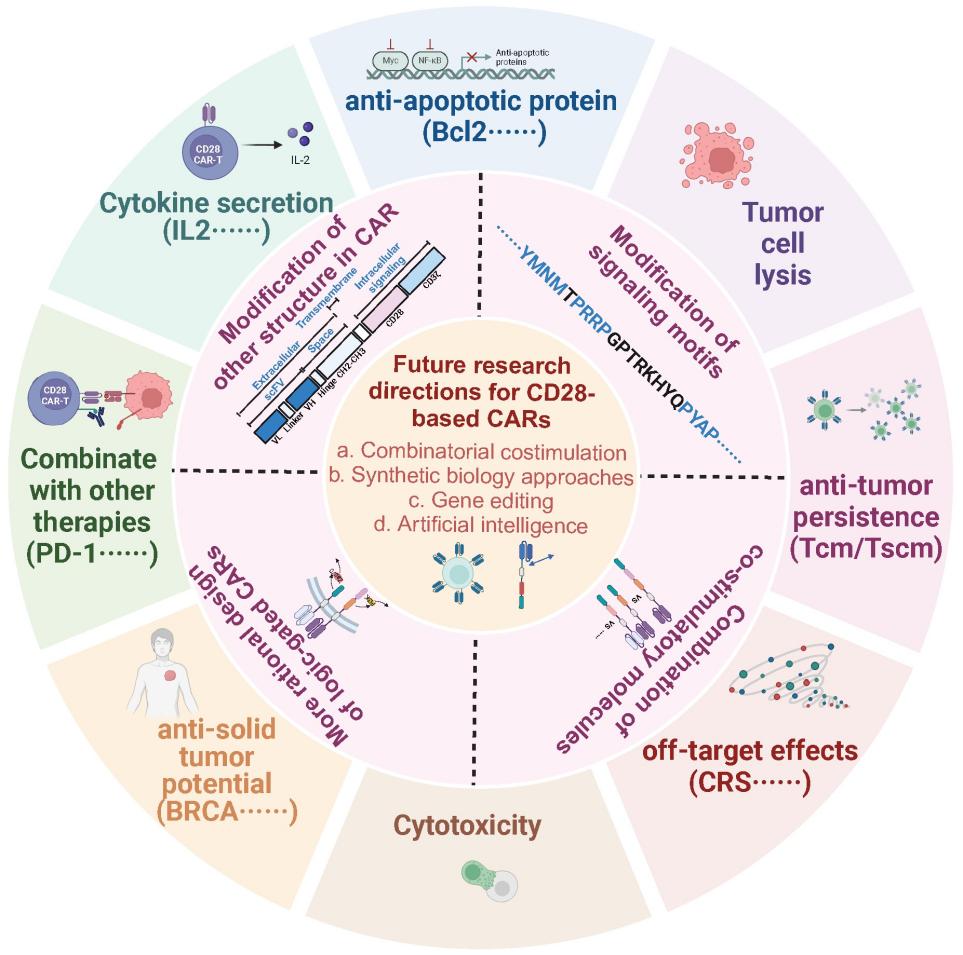
针对这些问题,研究人员总结了一系列基于CD28的CAR结构优化策略。在CD28信号基序优化方面,突变YMNM、PRRP和PYAP基序可降低T细胞耗竭和功能障碍,增强CAR-T细胞的持久性和抗肿瘤功效;分离CD28与CD3ζ信号,设计双靶CAR-T,可增强对双阳性肿瘤细胞的反应性,降低脱靶及肿瘤抗原逃逸风险;将CD28与其他共刺激分子组合,包括串联、并联及共刺激分子与配体组合模式,能实现优势互补,提升CAR-T细胞性能;优化CD28上下游结构域,如调整scFV与抗原结合亲和力、优化铰链区和跨膜结构域等,有望开发出整体性能更佳的CD28 CAR。优化策略有助于克服CD28-CAR T细胞存在的缺陷,提升CAR-T疗法在血液瘤和实体瘤治疗中的效果,为更多癌症患者带来希望。
本研究工作得到了国家自然科学基金、江苏省自然科学基金、江苏省高校自然科学研究计划等项目资助。
原文链接:https://doi.org/10.3389/fimmu.2025.1548772